Verónica Vizuete, Médico de Familia en el C.S. Puente Genil II y celiacas nos explica los métodos diagnosticos para la enfermedad celiaca
En el post anterior sobre la enfermedad celiacas (EC), hablamos sobre los distintos tipos de EC, la clínica de ésta enfermedad, sus signos y síntomas, distintos en la infancia y en la edad adulta, básico para el inicio del diagnóstico de la misma y por último hicimos distinción sobre la enfermedad celiacas, la alergia al gluten y la sensibilidad al mismo.
Una vez que el médico, bien por los síntomas y signos que presenta el paciente celiaco o porque proceda de un grupo de riesgo (por enfermedades asociadas o familiar de primer grado de un enfermo celiaco ya diagnosticado), éste debe en primer lugar solicitar una analítica para buscar los anticuerpos asociados a la EC.
Éste es un tema aún no muy conocido y difícil de explicar de forma simplificada y comprensible para todos los lectores, así que mis disculpas si algo quedó atrás o no es bien entendido.
Entre esa analítica, además de hemograma y bioquímica, el médico señala marcadores inmunológicos para detectar en la sangre del paciente con sospecha de EC como son los ANTICUERPOS asociados a la misma.
¿Qué son los anticuerpos, de dónde y por qué se producen?
Los anticuerpos (Ac), también conocidos como inmunoglobulinas (Ig), son una forma de proteína que pueden encontrarse en la sangre y otros fluidos corporales, empleados por el sistema inmunitario (sistema de defensa de nuestro organismo, como el sistema policial de una ciudad) para identificar y neutralizar elementos extraños tales como bacterias, virus, hongos y parásitos; son como nuestros policías internos. Los Ac son sintetizados por un tipo de leucocito denominado linfocito B (sargentos de la policía). Se conocen cinco tipos IgA, IgD, IgE, IgG e IgM. Difieren en: sus propiedades biológicas (como están hechos), localizaciones funcionales (donde van a defender) y capacidad para reconocer diferentes tipos de antígenos (moléculas reconocidas como extrañas y peligrosas para el organismo; como ya dijimos bacterias, virus, hongos y parásitos).
Pero los Ac se pueden producir también cuando el sistema inmunitario erróneamente considera el tejido sano como sustancia dañina. Esto se denomina “trastorno inmunitario”.
El gluten es una proteína amorfa que se encuentra en la semilla de muchos cereales (trigo, cebada, centeno, triticale, espelta y de forma controvertida en la avena) combinada con almidón. Representa un 80% de las proteínas del trigo y está compuesta de gliadina y glutenina. El gluten es el responsable de la elasticidad de la masa de harina, y confiere la consistencia elástica y esponjosa de los panes y masas horneadas. No indagaremos más sobre éste tema pues se ha hablado mucho ya en otras ocasiones.
La interacción entre genes de predisposición y factores ambientales (ambos aún no todos conocidos) desencadena una respuesta autoinmune inadecuada frente al gluten y prolaminas similares (grupo de proteínas vegetales con gran contenido en prolina, molécula similar a la gliadiana, que se encuentra en los cereales) en la mucosa del intestino delgado(1,2) en la que intervienen linfocitos T CD4+ específicos de la lámina propia. Sin embargo, antes de aparecer los anticuerpos en sangre, debe haber alteraciones tanto en la digestión intraluminal, como en la activación de mecanismos de la inmunidad innata en el epitelio y el trasporte trasepitelial de los péptidos proteicos (gliadina) (3).
El intestino es un tubo muy largo de 10 o 12 metros de largo en un adulto y tiene en su interior una capa simple de células (células absortivas o enterocitos), muy plegadas para que quepan formando pliegues (vellosidades y criptas). Estas son las células que nos defienden del enemigo exterior del ambiente; además de participar en la absorción de algunos nutrientes, previenen el paso descontrolado de sustancias, químicos, toxinas, macromoleculas que pueden entrar en nuestro cuerpo y, si lo hacen de manera descontrolada, podemos tener consecuencias clínicas severas. Como vemos en el dibujo del margen inferior derecho las células están unidas por algunas partes permitiendo el acceso de las sustancias nombradas por unos tipos de canales que se abren y cierran por corto período de tiempo en el que interviene una proteína que nuestro organismo fabrica llamada zonulina.
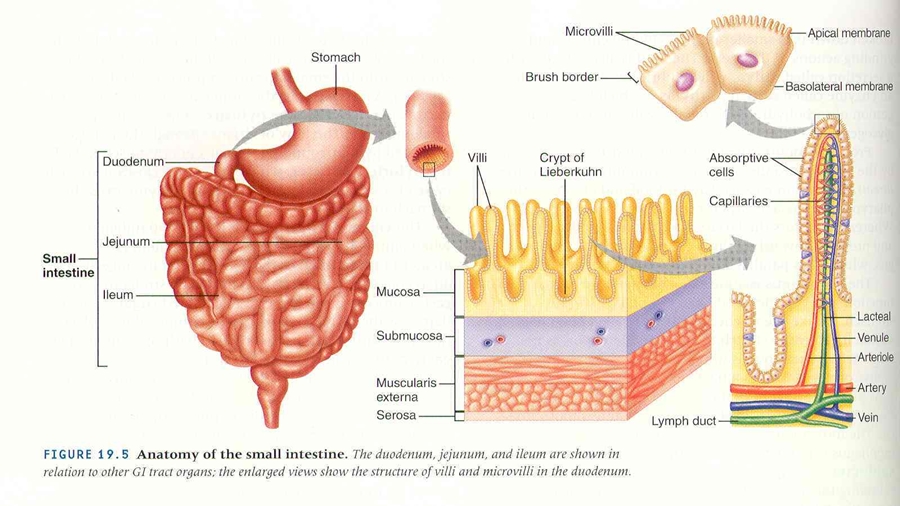
Fig. 1. Anatomía patológica o estructura del intestino delgado con sus componentes celulares y extracelulares que le dan la característica forma de borde de cepillo.
Cuando el control de estas entradas entre las células para el paso de sustancias no funciona bien, y en lugar de estar cerradas o casi cerradas, como tendrían que estar, están abiertas, sin control, hay sustancias que entran en el cuerpo y dependiendo de la predisposición genética que se tenga, se podrían desarrollar síntomas. En circunstancias normales, si estas entradas están cerradas, el gluten no debería entrar. Entonces, el primer paso para desarrollar la EC podría ser esta alteración en la digestión intraluminal (4).
En las personas con EC y otras muchas enfermedades autoinmunes se produce demasiada zonulina en momentos equivocados y, por tanto se produce una pérdida de la barrera intestinal que permite que moléculas, como el gluten, entren en el intestino y causen problemas si es que se presentan trastornos genéticos, en nuestro caso, predisposición genética para la EC.
En el celiaco, al entrar el gluten en la mucosa del intestino delgado, se produce una especie de alerta y como molécula no reconocida la estimulación de linfocitos y otras células de defensas para controlar los posibles daños que pueda ocasionar a los enterocitos o lámina propia (donde se asientan y se encuentran el resto de células y moléculas que forman la red que las sostienen).
En las fases iniciales o latentes de la enfermedad, los enterocitos no presentan cambios llamativos. Pero si se sigue ingiriendo gluten, se producela activación de mecanismos de la inmunidad innataponiéndose los linfocitos de la lámina propia en alerta ocurriendo una serie de acontecimientos entre los que destacamos:
– Aumento de los linfocitos intraepiteliales (LIE) y linfocitos T CD8+ y CD3+. De hecho, la primera anormalidad detectable de la EC es el aumento de los linfocitos T alfa-beta y LIE gamma-delta. “Son los policías específicos de la EC que acuden ante la alerta de la entrada de la gliadina/gluten(Antígeno) en nuestro organismo”. En respuesta se liberan citoquinas que promueven la inflamación, incluyendo interferón C, factor de necrosis tumoral y la interleucina 2; mediadores que hacen daño a nuestros propios enterocitos, ya que están entrenados para atacar al medio donde está el antígeno.
– Formación y liberación por parte de los linfocitos B de anticuerpos (serología):
- Anticuerpos Anti-Gliadina (AGA): son poco específicos (suele haber fasos positivos frecuentemente por infecciones como la giardiasis). Se siguen empleando en niños menores de 18 meses, ya que los niveles de otros anticuerpos, suelen ser negativos en dicho grupo de edad. Son muy útiles para el seguimiento, ya que se elevan pronto tras la ingesta de gluten. Los más informativos son los de la clase IgA (5).
- Anticuerpos Anti-Endomisio (AEM): realmente son anticuerpos anti-transglutaminasa tisular, pero determinados por inmunofluerescencia indirecta. Son muy específicos pero algo menos sensibles. La técnica es laboriosa y la interpretación subjetiva ya que depende del técnico que los valore por el microscopio. Los más informativos son los de la clase IgA (6).
- Anticuerpos Anti- Transglutaminasa tisular (ATGt): se valoran mediante una técnica objetiva que se llama ELISA. Los ATGt IgA puede que sean más adecuados que los AEM IgA para monitorizar la dieta (6); además, los AtTG se considera de gran importancia, ya que muestra una alta sensibilidad y especificidad y sus niveles se correlacionan con el grado de daño intestinal (7).
- Anticuerpos Anti-Peptido Deaminados de Gliadina (anti-DGP): dirigidos contra fragmentos de gluten, una vez han sido deaminados por el enzima transglutaminasa tisular, en el intestino. Se determinan también por ELISA. Más sensibles que los AEM, presentando una especificidad similar a los ATGt. Los más empleados son los de la clase IgG (5), por lo que pueden sustituir a los anti-tTG en pacientes con deficiencia selectiva de IgA (7).
Hay que tener en cuenta que las pruebas serológicas en el adulto, son bastante menos sensibles que en el niño, siendo sus resultados frecuentemente negativos (5).
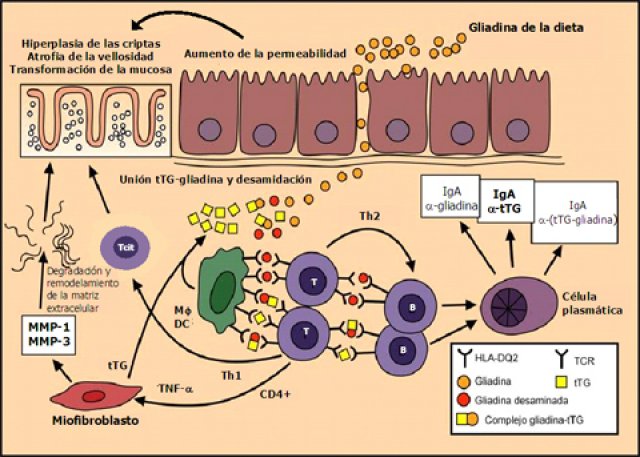
Fig. 2. Mecanismo fisiopatológico por el que el gluten en personas genéticamente predispuestas provocan una presentación errónea del gluten/gliadina para la formación de anticuerpos que no sólo atacan al mismo sino también a la estructura de la mucosa del intestino delgado provocando inflamación y aplanamiento de las vellosidades.
Pero ¿qué son los genes? ¿Y qué significa predisposición genética para la EC?
Los genes son unidades de almacenamiento de información genética, son segmentos de ADN que contienen la información sobre cómo deben funcionar las células del organismo. Tienen elementos que indican de dónde a dónde se tiene que leer (locus), y su contenido determina la composición de las proteínas que se forman. Los genes se encuentran en los cromosomas, heredados de nuestros padres, y éstos en cada una de las células de nuestro cuerpo humano. Los genes van a determinar cómo somos y nuestros rasgos y probables enfermedades a desarrollar, aunque también los genes pueden sufrir alteraciones o modificaciones que no tenían previamente.
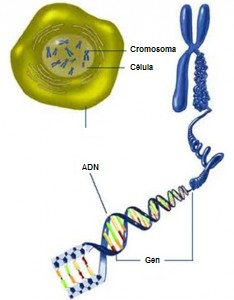
En el caso que nos ocupa, la EC, en el cromosoma número 6 (de los 46 que tenemos en cada célula), se cree que se ha producido una alteración en un “locus” que fabrica unas proteínas, HLA, que están presentes en las membranas (cubierta exterior) de casi todas las células del organismo, especialmente los leucocitos, entre ellos los linfocitos B (como se ve en la figura 2), presentando al gluten al resto de las células de defensas como un antígeno (cuerpo extraño) y provocando la formación de anticuerpos.
Los médicos y científicos la localizan en nuestros genes por la posición que ocupan en ese cromosoma 6, denominándose HLA- DQA1*0501-DQB1 *0201 pues está presente en el 93% de las personas celiacas (o bien, en lugar de *0201, *0202). Y estos genes son los que codifican la molécula llamada DQ2. Se sabe también que el 4% de las personas celiacas tienen estos dos genes: HLA DQA1 *0301 – DQB1 *0302, que codifican la molécula que se llama DQ8. Esto quiere decir que casi todas las personas celiacass tienen o bien DQ2 o DQ8 y que, por lo tanto, es muy raro que una persona sea celiaca si no tiene uno u otro. Se podría pensar entonces, deducirse, que quien tenga DQ2 o DQ8 es celiaco, y el que no tenga ni uno ni otro, no lo es. Pero no es así ya que hay personas celiacass, que lo son sin ninguna duda, y que no tienen ni DQ2 ni DQ8 (el 2%-3% de la población celiaca). Además el 20% de la población que no es celíaca tiene DQ2 y no han padecen de EC. Estos están predispuestos a padecer la EC, según factores ambientales y otros factores aún no conocidos (tienen la genética pero no desarrollan la enfermedad).
En algunos Centros de Salud se puede solicitar el estudio de genético asociado a la EC, sobre todo a familiares de primer grado de un paciente celíaco o del grupo de alto riesgo. Pero no todos cuentan en España con éste recurso, entonces sería a criterio del especialista o el analista el que según la sospecha clínica o resultados analíticos de los anticuerpos, lo solicitarán y/o realizarán o no. Nos sirve sobre todo para excluir la EC si no están presentes ni HLA-DQ2 ni HLA-DQ8.
Tras la sospecha de EC el Médico de Familia o Pediatra solicitará una analítica (serología), es imprescindible hasta el diagnóstico final, mientras sea posible ,que en todo momento se siga una dieta CON GLUTEN, ya que el modificar la dieta podría alterar los resultados y confundir al personal médico que los interpreta para un diagnóstico correcto.
En Gastroenterología pediatríca, si la clínica es típica, los ATGt claramente positivos (>10 veces la normalidad), HLA- DQ2 o DQ8 positivo, podría excluirse la biopsia intestinal, máxime aún si la respuesta a una dieta sin gluten normaliza síntomas y alteraciones analíticas (8).
Sin embargo, en las formas subclínicas de la enfermedad y en el adulto, no pueden ser utilizados como único criterio diagnostico; la endoscopia o biopsia mediante cápsula de Crosby digestiva alta sigue siendo en estos casos la prueba de oro. En tal caso el Gastroenterólogo que realice la prueba deberá conseguir al menos 5 muestras y una de ellas en bulbo. Es muy importante tener en cuenta la orientación de la muestra y las características de las vellosidades. La valoración histológica deberárealizarse de acuerdo con los criterios de Marsh-Oberhuber (8)
Éstos criterios nos informan del grado de lesión (inflamación) de la mucosa intestinal en el momento de realizarla y puede ser de tipo 1, tipo 2 y tipo 3ª(3ª, 3b o 3c). Pero no guarda ninguna relación con el grado de tolerancia al gluten; el que es diagnosticado como celiaco debe hacer, independientemente de los criterios de Marsh, una dieta estricta sin gluten de por vida para evitar complicaciones y enfermedades asociadas además de la recuperación de las vellosidades intestinales.
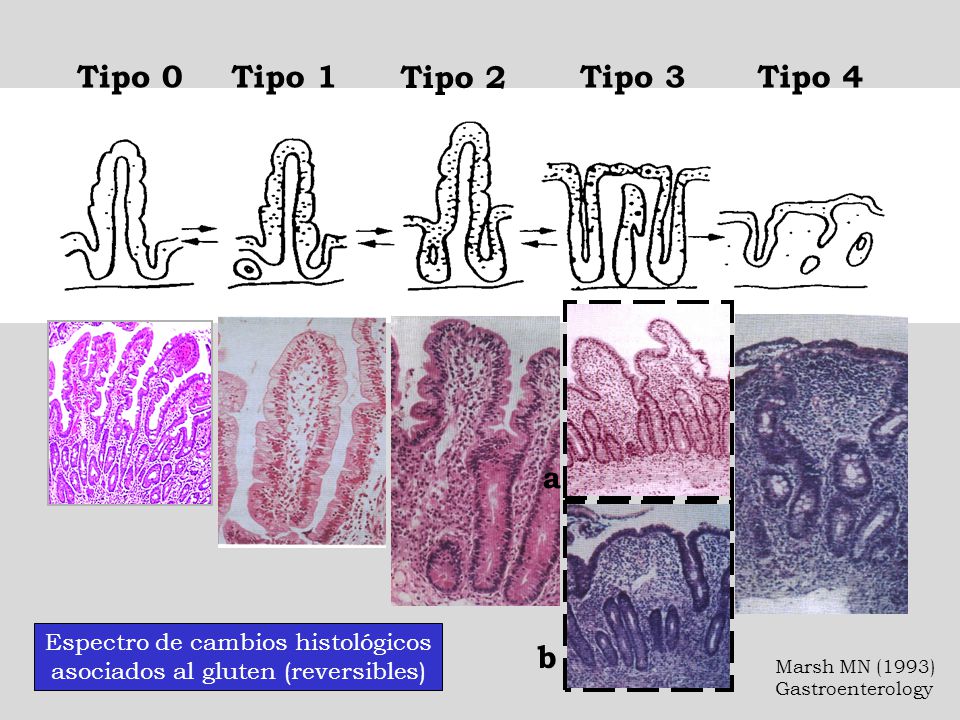
Si el centro además donde se realice el análisis anatomopatológico está además dotado para hacer estudio inmunohistoquímico (clase de linfocitos y proporción que hay en la lámina propia de la muestra que se extraiga), ayudaría mucho a los diagnósticos con sospecha.
Como podemos ver, el diagnóstico de la EC no es nada fácil, la clínica es variable, los anticuerpos que se determinan no son del todo sensibles ni específicos, y a veces la endoscopia no se puede realizar correctamente y las muestras que se obtienen, si se cogen en períodos muy incipientes de la enfermedad pueden no ser concluyentes…entonces sería importante si existe clínica compatible con EC hacer estudio genético e inmunohistoquímico.
En la siguiente edición pondremos algunos casos clínicos, podremos resolver dudas y hablaremos del seguimiento de la enfermedad celiaca.
BIBLIOGRAFÍA
-
Jabri B, Kasarda DD, Green PH. Innate anda adaptative inmunity: the yin and yang of celiac disease. Inmunol Rev 2005;206:219-31.
-
Ciccocioppo R, Di Sabatino, Corazza GR. The inmune recognition of fluten in coeliac disease. Clin Exp Inmunol 2005;140:408-16.
-
Arranz E, Garrote JA. Enfermedad Celíaca: introducción al conocimiento actual de la enfermedad celíaca; capítulo 12, 169.
-
FARESTAIE- INSTITUTO DE ANÁLISISNoticias para Profesionales. Enfermedad Celíaca – Entrevista al Dr. Alessio Fasano. Gastroenterólogo pediátrico de los Estados Unidos, quien explica la definición, diagnóstico y diferencias entre enfermedad celíaca, sensibilidad al gluten y alergia al trigo.
-
Arranza E, Bode J, kigestone K, Ferguson A. Intestinal antibody pater of celiac disase: asociaton with gamma/delta T cell receptor expresión by intrepithelial lymphocytes, and other índices of potential coeliac disease. Gut 1993;105:901-5.
-
Ruiz-Diaz A, Polanco I. Exposición al gluten y aparición de enfermedades autoinmunes en la enfermedad eclíaca. Pediatrika 2002;22:311-9.
-
Sategna C. Solerio E, Scaglione N, Aimo G, Mengozzi G. Duration of gluten exposure in adult celiac disease does not correlate with the risk for autoinmune disorders. Gut 2001;49:502-5.
-
Vitoria JC, Bilbao, JR. Novedades en enfermedad celíaca. An Pediatr.2013;78:1-5 – Vol. 78 Núm.1 DOI: 10.1016/j.anpedi.2012.09.002